Kho Kiến Thức
Công thức tính số mol, nồng độ mol & nồng độ phần trăm (C%) có bài tập – Tin Công Nghệ
1️⃣ Công thức tính số mol, nồng độ mol & nồng độ phần trăm (C%) có bài tập – Tin Công Nghệ ✔️
1. Số mol là gì?
– Số mol hay mole (kí hiệu mol) là công ty đo đạc dùng trong hóa học là lượng chất có chứa xấp xỉ 6,022.10 23 nguyên tử hoặc phân tử của chất đó.
– Con số 6,022.10 23 được xem là hằng số Avogađro (kí hiệu N).
Số mol trong hóa học là gì?
2. Các công thức tính số mol
Tính số mol qua khối lượng
Đối với tình huống đề bài cho biết trọng lượng của 1 chất hoặc hợp chất, ta tính số mol bằng công thức sau:
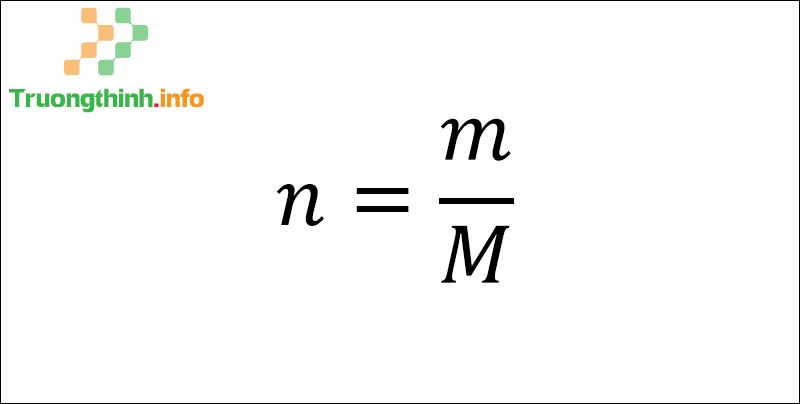
Công thức tính số mol qua khối lượng
Trong đó :
Tính số mol qua thể tích
Đối với trường hợp đề bài cho thấy thể tích của một chất, hợp chất khí, ta tính số mol bằng công thức sau:
– Ở điều kiện chỉ tiêu (đktc) :
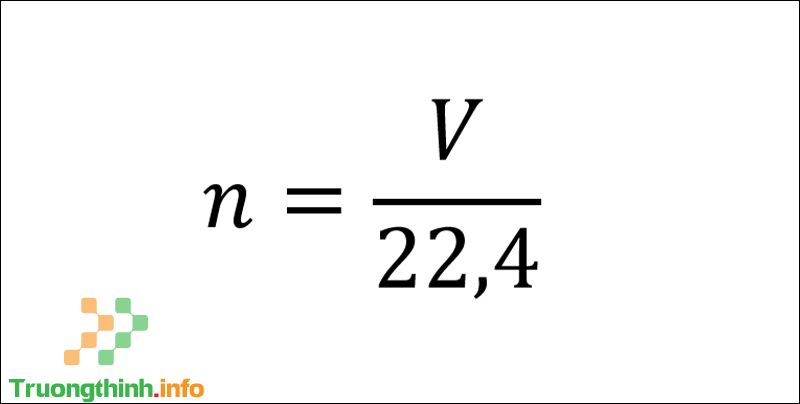
Công thức tính số mol qua thể tích ở đktc
Trong đó :
– Ở điều kiện thường :

Công thức tính số mol qua thể tích ở điều kiện thường
Trong đó :
Tính số mol qua số Avogadro
Đối với trường hợp đề bài cho thấy số nguyên tử hoặc phân tử của một chất hoặc hợp chất, ta tính số mol bằng công thức sau:

Công thức tính số mol qua số Avogadro
Trong đó :
Tính số mol qua nồng độ mol
Đối với tình huống đề bài cho biết nồng độ mol và thể tích của một dung dịch, ta tính số mol bằng công thức sau:
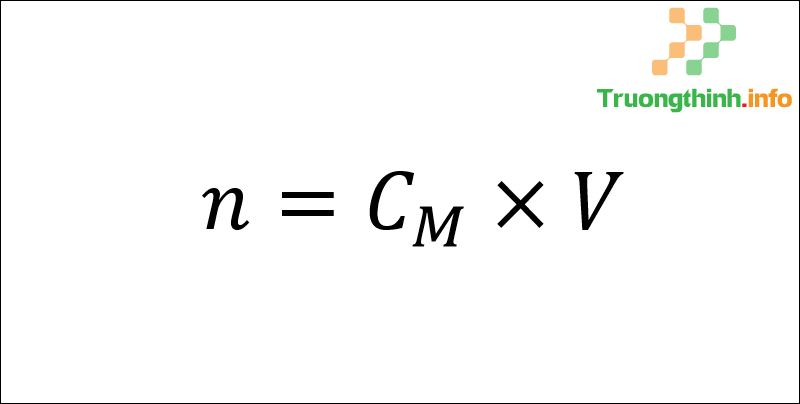
Công thức tính số mol qua nồng độ mol
Trong đó :
Tính số mol qua nồng độ phần trăm
Đối với trường hợp đề bài cho biết nồng độ phần trăm (C%) và cân nặng của dung dịch sau phản ứng, ta tính số mol bằng công thức sau:

Công thức tính số mol qua nồng độ phần trăm
Trong đó :
Tính số mol qua khối lượng riêng
Đối với tình huống đề bài cho thấy khối lượng riêng , thể tích dung dịch và nồng độ phần trăm (C%) của dung dịch, ta tính số mol bằng công thức sau:
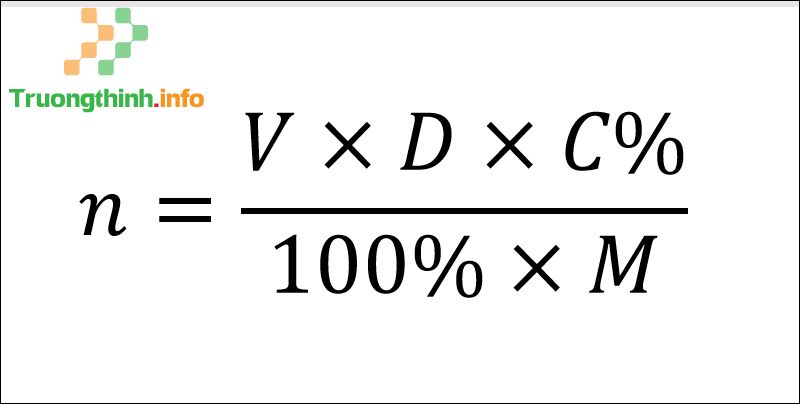
Công thức tính số mol qua cân nặng riêng
Trong đó :
3. Cách tính số mol dư
Trong tình huống đề bài đòi hỏi xác định chất còn dư sau phản ứng . Lúc này ta tính số mol theo công thức sau:
4. Công thức tính nồng độ phần trăm (C%) của dung dịch
Khái niệm nồng độ phần trăm
Nồng độ phần trăm (C%) của dung dịch là đại lượng bộc lộ số gam chất tan có trong 100 gam dung dịch.
Kí hiệu : C%.
Đơn vị : %.
Công thức tính nồng độ phần trăm
Để tính nồng độ phần trăm (C%) ta áp dụng công thức sau:
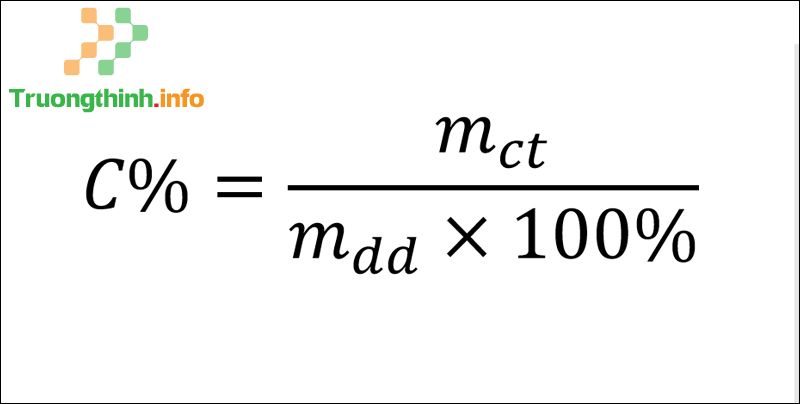
Công thức tính nồng độ phần trăm
Trong đó :
Ví dụ cách tính nồng độ phần trăm (C%) của dung dịch
Cho bài tập tỉ dụ sau : Cho dung dịch H 2 SO 4 có nồng độ 28%. Tính khối lượng H 2 SO 4 có trong 300g dung dịch.
Hướng dẫn giải :
Khối lượng của H 2 SO 4 có trong 300g dung dịch:

Hướng áp giải
5. Công thức tính nồng độ mol (CM) của dung dịch
Khái niệm nồng độ mol
Nồng độ mol của dung dịch là đại lượng bộc lộ số mol chất tan có trong 1 lít dung dịch.
Kí hiệu : C M .
Đơn vị : mol/l hoặc M.
Công thức tính nồng độ mol
Để tính nồng độ mol của dung dịch ta áp dụng công thức sau:
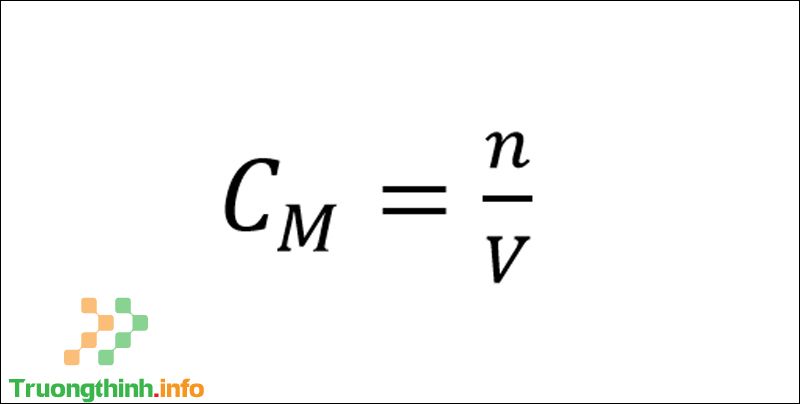
Công thức tính nồng độ mol
Trong đó :
Ví dụ phương pháp tính nồng độ mol (CM) của dung dịch
Cho bài tập tỉ dụ sau : Trộn 1 lít dung dịch đường 2M với 3 lít dung dịch đường 0.5M. Tính nồng độ mol của dung dịch đường sau khi trộn vào nhau.
Hướng dẫn giải :

Hướng dẫn giải
6. Bảng công thức đầy đủ về tính số mol, nồng độ mol, nồng độ phần trăm

Bảng công thức đầy đủ
7. Bài tập tính số mol, nồng độ phần trăm (C%) và nồng độ mol (CM) của dung dịch
Bài tập tính số mol
Câu 1 : Khối lượng mol chất là:
A. Là khối lượng sau khi tham gia phản ứng hóa học.
B. Bằng 6.10.
C. Là trọng lượng tính bằng gam của N nguyên tử hoặc phân tử chất đó.
D. Là khối lượng ban đầu của chất đó.
Đáp án : D.
Câu 2 : Cho biết 1mol chất khí ở điều kiện bình thường có thể tích là:
A. 2,24 lít.
B. 0.224 lít.
C. 22,4 lít.
D. 22,4 ml.
Đáp án : C.
Câu 3 : Tính thể tích ở đktc của 2,25 mol O2.
A. 22,4 lít.
B. 24 lít.
C. 5,04 lít.
D. 50,4 lít.
Đáp án : D.
1 mol ở đktc là 22,4 l ⇒ 2,25mol là 2,25 x 22,4 = 50,4 (lít).
Câu 4 : Tính nồng độ mol của dung dịch khi hòa tan 15,8g KMnO4 trong 7,2 lít nước.
Đáp án :

Đáp án câu 4
Câu 5 : Tính số mol nguyên tử hoặc phân tử trong các lượng chất sau: 1,44.10 23 phân tử HCl.
Đáp án :
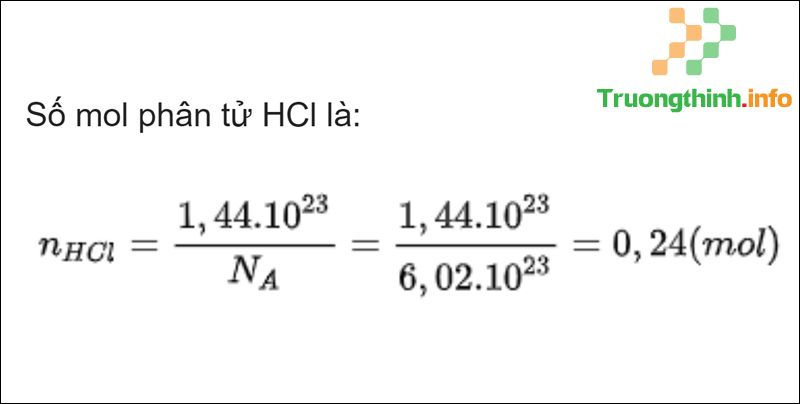
Đáp án câu 5
Bài tập tính nồng độ mol (CM)
Câu 1 : Số mol trong 400ml NaOH 6M là:
A. 1,2 mol.
B. 2,4 mol.
C. 1,5 mol.
D. 4 mol.
Đáp án : B.
n = 0.6 x 4 = 2,4 (mol).
Câu 2 : Hòa tan 300ml Ba(OH) 2 0,4M. Tính khối lượng của Ba(OH) 2 .
A. 20,52 gam.
B. 2,052 gam.
C. 4,75 gam.
D. 9,474 gam.
Đáp án : A.
+ n Ba(OH) 2 = 0,4 x 0,3 = 0,12 mol.
+ m Ba(OH) 2 = 0,12 x 171 = 20,52 gam.
Câu 3 : Tính nồng độ mol của 456 ml Na 2 CO 3 10,6 gam.
Đáp án : D.
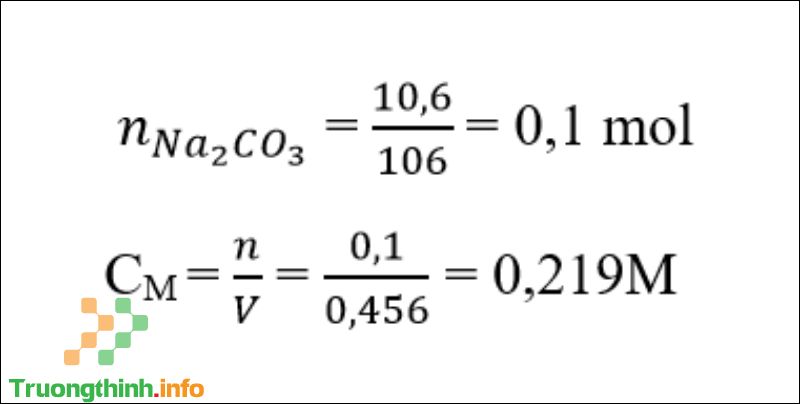
Đáp án câu 3
Câu 4 : Dung dịch HCl 25% (D = 1,198g/ml). Tính C M .
A. 8M.
B. 8,2M.
C. 7,9M.
D. 6,5M.
Đáp án : B.

Đáp án câu 4
Câu 5 : Trong 200ml dung dịch có hòa tan 16g NaOH. Tính nồng độ mol của dung dịch.
Đáp án :

Đáp án câu 5
Bài tập tính nồng độ phần trăm (C%)
Câu 1 : Hòa tan 40% trong 90g dung dịch. Số mol cần tìm là.
A. 0,225 mol.
B. 0,22 mol.
C. 0,25 mol.
D. 0,252 mol.
Đáp án : A.
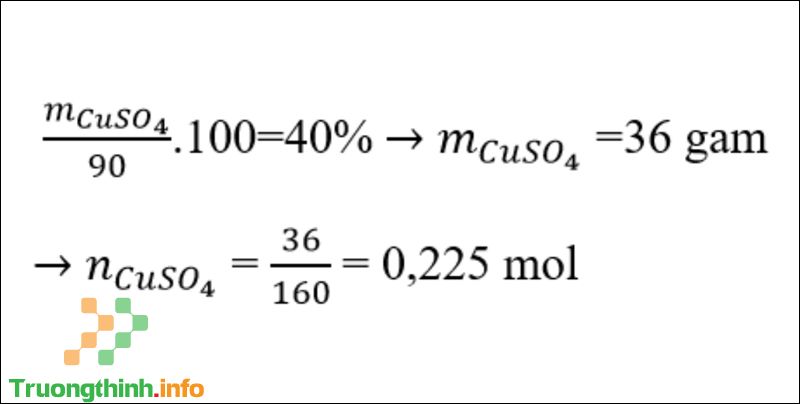
Hướng áp giải câu 1
Câu 2 : Dung dịch NaOH 4M (D = 1,43 g/ml). Tính C%.
A. 11%.
B. 12,2%.
C. 11,19%.
D. 11,179%.
Đáp án : C.

Hướng áp giải câu 2
Câu 3 : Hòa tan 40g đường với nước được dung dịch đường 20%. Tính khối lượng dung dịch đường thu được.
A. 150 gam.
B. 170 gam.
C. 200 gam.
D. 250 gam.
Đáp án : C.

Hướng dẫn giải câu 3
Câu 4 : Hòa tan 50g đường với nước được dung dịch đường 10%. Tính khối lượng nước cần cho pha trộn dung dịch.
A. 250 gam.
B. 450 gam.
C. 50 gam.
D. 500 gam.
Đáp án : B.

Hướng dẫn giải câu 4
Câu 5 : Chọn lời đáp đúng: Bằng cách nào ta có được 200g dung dịch BaCl 2 5%?
A. Hòa tan 190g BaCl 2 trong 10g nước.
B. Hòa tan 10g BaCl 2 trong 190g nước.
C. Hòa tan 100g BaCl 2 trong 100g nước.
D. Hòa tan 200g BaCl 2 trong 10g nước.
Đáp án : B.
8. Một số lưu ý để làm tốt bài tập
– Cần thuộc các công thức về tính số mol, nồng độ mol, nồng độ phần trăm.
– Rèn luyện kỹ năng viết phương trình.
– Chú ý các công ty trong bài đã đúng hay chưa.
– Sử dụng máy tính cầm tay để có kết quả nhanh và chính xác hơn.

Một số lưu ý
– Đọc thật kỹ đề bài để không bỏ qua những dữ liệu quan trọng.
– Thường xuyên làm bài tập, giải đề để rèn dũa khả năng và tốc độ giải bài tập.
Một số mẫu Máy tính cầm tay Flexio đang mua bán tại Chúng tôi:
Trên đây là bài viết về công thức tính số mol, nồng độ mol, nồng độ phần trăm trong hóa học. Rất mong bài viết sẽ được ích đối với bạn và hẹn tái ngộ ở những bài viết sau!
công thức tính số mol,công thức tính nồng độ mol,công thức tính nồng độ phần trăm,công thức,cách tính
Nội dung ✔️ Công thức tính số mol, nồng độ mol & nồng độ phần trăm (C%) có bài tập – Tin Công Nghệ được tổng hợp sưu tầm biên tập bởi 1️⃣❤️: Trường Thịnh Group. Mọi ý kiến vui lòng gửi Liên Hệ cho truongthinh.info để điều chỉnh. truongthinh.info tks.





